Il concetto di purezza non è altro che una idealizzazione perché tutto è imperfetto. Anche se dovesse mai nascere qualcosa di puro esso verrebbe istantaneamente contaminato e perderebbe dunque la sua purezza. L’acqua non fa eccezione e dunque la domanda è lecita: ha senso studiare tanto approfonditamente l’acqua pura se, in pratica essa la troviamo sempre mista a particelle in sospensione/soluzione, o con gas disciolti al suo interno o contaminata in altro modo?
Proviamo ad approfondire il comportamento dell’acqua in presenza di altre sostanze cominciando con l’acqua salata del mare e che costituisce una quota importante del liquido amniotico.
Il sale da cucina contenuto nell’acqua di mare è quasi totalmente costituito da ioni sodio e ioni cloro che si combinano per dare il Cloruro di sodio NaCl e lo si ottiene molto facilmente come residuo solido facendo banalmente evaporare l’acqua. Utilizzando il metodo semplificato dell’elettronegatività già utilizzato in precedenza per l’acqua(1), dalla tabella di Henry otteniamo per il sodio EN0(Na)=1,01 e per il cloro EN0(Cl)=2,83 e applicando le formule già viste in precedenza(1) otteniamo:
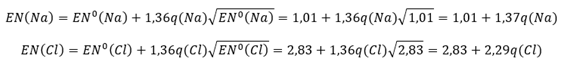
Per il principio di conservazione della carica abbiamo q(Na) + q(Cl) = 0 e per la molecola di cloruro di sodio vale la relazione EN(Na) = EN(Cl) = EN(NaCl).
Facendo i calcoli otteniamo: EN(NaCl) = 1,70 q(Na) = +0,50 e q(Cl) = -0,50.
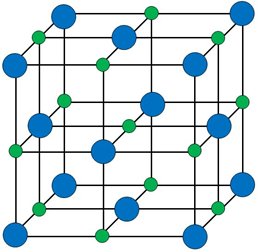
Eseguiamo il medesimo calcolo per l’HCl ricordando che per l’idrogeno dalla tabella di Henry troviamo EN0(H) = 2,1 e per il cloro abbiamo q(Cl) = -0,17. Come si vede, la differenza di elettronegatività è assai rilevante: -0,50 contro -0,17; è questo il motivo per il quale l’atomo di cloro piuttosto che unirsi a quello di idrogeno per dare origine ad un gas maleodorante come l’acido cloridrico (HCl), predilige unirsi a quello di sodio dando vita ad un cristallo solido a struttura cubica(2). Tenendo conto che nel cloruro di sodio allo stato di vapore, la distanza fra atomo di sodio e atomo di cloro è circa pari a 2,36 Å, applicando la legge di Coulomb si trova un’energia elettrostatica pari a -35 kcal/mol(3), cioè quasi il triplo di quella relativa al legame a idrogeno(4). Si tratta dunque di un legame che rimane molto stabile anche ad alte temperature.
Le cose cambiano radicalmente se gettiamo il sale in acqua. Immaginiamo idealmente di poter avvicinare una molecola d’acqua ad una di cloruro di sodio sufficientemente da ottenere una molecola NaClH2O, cioè tanto vicino che la nuvola elettronica ronzi attorno all’insieme di tutti gli atomi costituenti questa nuova “molecola”. Applicando il nostro metodo a questo nuovo insieme di atomi otteniamo:
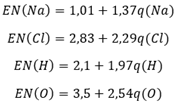
Anche in questo caso, per il principio di conservazione della carica abbiamo q(Na) + q(Cl) + 2q(H) + q(O) = 0 e anche per questa nuova “molecola” vale la relazione EN(Na) = EN(Cl) = EN(H) = EN(O) = EN(NaClH2O) in quanto siamo partiti da due molecole – quella dell’acqua e quella del cloruro di sodio – entrambe neutre.
Il risultato è EN(NaClH2O) = 2,13 q(Na) = +0,82 q(Cl) = -0,31 q(H) = +0,02 q(O) = -0,54.
Constatiamo che il valore di q(Na) è cresciuto notevolmente passando da +0,50 a +0,82. Se aggiungiamo altre molecole d’acqua all’insieme e rifacciamo i calcoli per una ipotetica “molecola” NaCl(H2O)n costituita da una molecola di cloruro di sodio e “n” molecole d’acqua, all’aumentare del numero di molecole d’acqua otteniamo un progressivo aumento del valore di q(Na) fino superare +1,0 (=2×0,5), valore tale da rendere più conveniente per il sodio associarsi all’acqua piuttosto che al cloro(5). Per sapere quanto vale “n” affinchè q(Na) ≥ +1 basta applicare la formula q(Na) + q(Cl) + 2nq(H) + nq(O) =0.
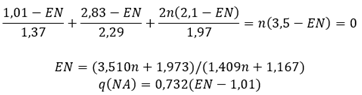
A calcoli fatti risulta un valore di “n” compreso fra 4 e 5, molto vicino a 5, il che significa che quando il rapporto fra molecole di H2O e NaCl supera 5, il sodio preferirà unirsi alle molecole di acqua piuttosto che associarsi al cloro. Tenendo conto che il cloruro di sodio ha massa molecolare pari a 58,44 g/mol e che l’acqua ha 18,02 g/mol, se in una pentola versiamo cento grammi di sale da cucina in 1.000 grammi d’acqua e poi accendiamo il fornello per far evaporare l’acqua, finchè l’acqua liquida non si ridurrà a soli 154 grammi non assisteremo alla precipitazione del sale sottoforma di cristalli solidi. In altre parole, il sale da cucina è talmente solubile in acqua che basta un rapporto in peso di 2:3 per avere completa solubilità.Raccontato in altre parole, le molecole d’acqua, organizzate in gruppetti, circuiscono gli atomi di sodio invitandoli a interrompere il loro rapporto monogamico col cloro per passare ad un rapporto poligamico. Per far ciò le molecole d’acqua circondano letteralmente il sodio come farebbe un gruppo di invitanti sirene che, per essere sempre più convincenti aumentano via via di numero finchè non riescono a “convincere” il malcapitato atomo di sodio a tradire il cloro e a cominciare una relazione “orgiastica” con loro. A quel punto il sodio, circondato dalle molecole d’acqua, non può far altro che abbandonare il cloro e farsi circuire dalle molecole d’acqua. I chimici chiamano questo fenomeno solvatazione.
Torino 19 gennaio 2020
Gianfranco Pellegrini
Note
(1) Vedi l’articolo precedente “La chimica semplice applicata all’acqua”.
(2) Come mostra la figura sottoriportata, nel cristallo di cloruro di sodio ogni atomo di sodio è circondato da sei atomi di cloro e viceversa, ogni atomo di cloro è circondato da sei atomi di sodio.
(3) Partendo dalla formula E = e2q1q2/(4πε0r) (con r espresso in Å) e ponendo e2/4πε0 = 332, r= 2,36, q1 = +0,50 e q2 = -0,50, otteniamo E = -35 q1q2/r = [kcal/mol].
(4) Vedi l’articolo precedente “La chimica semplice applicata all’acqua”.
(5) Il grafico sottostante mostra l’aumento asintotico dell’elettronegatività del sodio all’aumentare delle molecole d’acqua vicine all’atomo. Si vede facilmente che quando abbiamo più di 5 molecole d’acqua per ogni molecola di cloruro di sodio, il sodio si scombina dal cloruro di sodio e si associa all’acqua.

