In questo articolo scopriremo la grande capacità dell’acqua ad adattarsi al tipo di soluto con cui reagisce.
Prendiamo come esempio il catione Cl7+, ossia l’atomo di cloro privato dei sette elettroni più esterni e analizziamo il suo comportamento in acqua pura. Si tratta di un atomo di piccole dimensioni(1) e dunque potrà essere solvatato al massimo da quattro molecole d’acqua:
Cl7+ + 4 H2O –> [Cl(H2O)4]7+
Applicando le regole che abbiamo imparato ad utilizzare negli articoli precedenti e facendo uso della tabella di Henry, otteniamo:

q(H) = 0,507(EN + 2,1) = +0,80
Si tratta del quadruplo del q(H) per l’acqua pura (+0,20); il livello di polarizzazione del legame O – H da parte del soluto risulta talmente elevato che, piuttosto che solvatare lo ione Cloro, il protone preferirà legarsi all’acqua mediante legame O – H, il cui q(H) è decisamente minore q(H) = +0,32(2).
I chimici chiamano “idrolisi”(3) questa fuga dei protoni dal nucleo centrale A) di solvatazione verso la zona B)(4). Per sapere quando un tale processo si arresta basta riprendere la formula che mette in relazione l’elettronegatività con in pH(5):
EN(H2O) = 2,732 – 0,035pH (2)
Il processo si arresterà quando il pH relativo al catione idrolizzato eguaglierà quello relativo al catione non idrolizzato. Per effettuare questo calcolo generalizziamo la formula (1) soprariportata:

Dove “n” rappresenta il numero di protoni perduti dalla specie [Cl(H2O)4]7+ che dunque diventa [Cl(H2O)4](7-n)+.
Eguagliando la (2) e la (3) si ottiene:
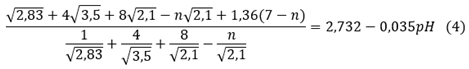
Da cui si ricava:

Nelle condizioni di massima acidità (pH≈0), si trova n= 8,3 > 8. Questo valore ci indica inequivocabilmente che anche in condizioni di acidità estrema la zona di solvatazione dello ione Cl7+ (zona A) risulterà priva di protoni. Queste considerazioni ci permettono di concludere che nella soluzione, piuttosto che cationi Cl7+ troveremo anioni ClO4–. In effetti è esattamente ciò che si ritrova in pratica; l’approccio lagrangiano ci ha consentito di verificare con calcoli semplici il fatto sperimentale.
Generalizzando il concetto possiamo concludere che, in queste condizioni, l’acqua in zona A) perde completamente le sue capacità anioniche e mantiene esclusivamente quelle cationiche. L’esempio che abbiamo approfondito in questo articolo mostra come l’acqua sia in grado di adattarsi meravigliosamente al tipo di soluto col quale si trova a coesistere.
Torino 15 marzo 2020
Gianfranco Pellegrini
Note
(1) Il suo raggio atomico è pari a circa 0,2 Ångström.
(2) Come abbiamo visto nell’articolo precedente “Relazione fra elettronegatività e pH per l’acqua”, abbiamo visto che il legame O – H corrisponde a [H+, (H2O)2] equivalente a [H5O2]+ con EN = 2,732 e q(H) = 0,507(EN – 2,1) = +0,32.
(3) In formule si può scrivere:
[Cl(H2O)4]7+ + 2H2O –> [ClOH(H2O)3]6+ + [H2O]+
Facendo gli stessi calcoli dell’EN fatti per [Cl(H2O)4]7+ si ottiene per il catione idrolizzato EN[Cl(H2O)4]7+ = 3,63 contro un valore di 3,67 per il catione non idrolizzato [ClOH(H2O)3]6+. Se si continuano a sottrarre protoni si arriva ad un valore minimo di EN pari a 2,86 corrispondente all’anione [ClO4]+ (ione iperclorato).
(4) Come visto nella nota 3) dell’articolo precedente “Potere solvatante dell’acqua”, l’acqua in presenza di soluto è composta di nuclei di solvatazione (zona A che i chimici chiamano “sfera di coordinamento”), circondati da acqua pura (zona C) e, tra zona A) e zona C), esiste una zona B) di interfaccia in cui le molecole d’acqua subiscono l’influenza sia da parte delle molecole della zona A), sia di quelle imperturbate della zona C).
(5) Vedi l’articolo precedente “Relazione fra elettronegatività e pH per l’acqua”.
